丝素蛋白(silk-fibroin,SF)虽然具有良好的生物学特性,但由于其降解速度较快,力学性能较差,在长距离血管缺损修复中受到极大的限制。因此,有必要构建一种基于SF的多功能复合支架。在这项研究中,通过改进的渗透法制备了一种新型磁性SF支架(MSFC)。与SF支架(SFC)相比, MSFCs具有更好的结晶性、磁热性能和机械强度,这主要归因于铁基磁性纳米颗粒(MNPs)的合理引入。此外,体内外实验表明,MSFCs的降解性显著延迟。延迟降解的机理是SFC与MNPs之间形成新的氢键和其内部的铁原子与酪氨酸络合(蛋白水解酶的活性中心)抑制水解酶活性的双重作用。进一步研究证明,随着铁浓度的升高,MSFCs中的β-折叠含量增加,证明了MNPs掺杂后更有利于丝素蛋白向结晶化序列转变。此外,虽然巨噬细胞可以吞噬释放的MNPs,但并不影响其功能性,甚至合理的水平也能引起细胞因子的上调。体内外的研究表明,MSFCs具有良好的生物相容性,且对CD34标记的血管内皮细胞 (VECs)具有生长促进作用。总之,我们证实了MNPs的掺杂可以显著延迟SFC的降解,从而为多功能生物复合材料在组织工程中的应用提供了新的视角。
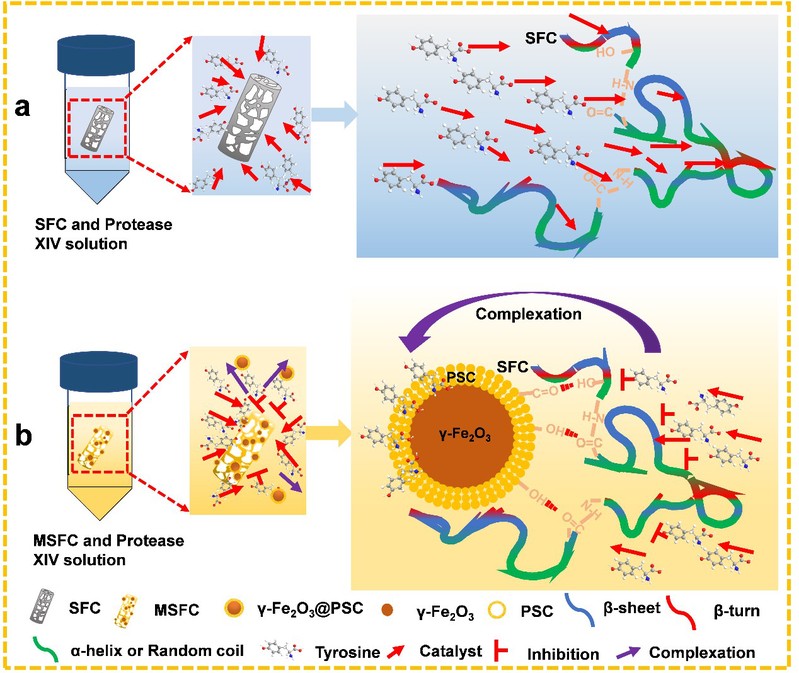
SFC延缓降解机制:MNPs与SFC形成新的氢键协同铁原子络合酪氨酸(蛋白酶的活性中心)抑制蛋白酶活性,两者协同作用延缓SFC的降解。
该论文已经在线发表在Bioactive Materials上,具体信息如下:
Xin Liu, Yuxiang Sun, Bo Chen, Yan Li**, Peng Zhu, Peng Wang, Sen Yan, Yao Li, Fang Yang***, Ning Gu*. Novel magnetic silk fibroin scaffolds with delayed degradation for potential long-distance vascular repair,Bioactive Materials, 2021.https://doi.org/10.1016/j.bioactmat.2021.04.036
论文下载链接:https://authors.elsevier.com/sd/article/S2452-199X(21)00212-7