癌症一直威胁人类健康,是人类长寿路上的绊脚石。如何有效治疗一直是科学家探索的方向。靶向诊疗探针的出现为肿瘤诊治打开了一扇新的大门,精确设计的探针可增强其体内药物代谢效率、靶向性和疗效。利妥昔单抗是一种应用于临床长达30年的商业化抗体,已经延长甚至拯救了无数生命。但是,由于潜在的耐药性和副作用,仍旧有许多患者无法从利妥昔单抗中受益。
基于此,本文制备了13nm的磁性纳米探针——利妥昔单抗标记的氧化铁纳米颗粒Fe3O4@DMSA@Ab,其中的磁核为2,3-二巯基丁二酸修饰6.5nm的氧化铁纳米颗粒Fe3O4@DMSA,交联剂(碳二亚胺EDC/磺酸化-N-羟基琥珀酰亚胺丙烯酸酯)作用下将利妥昔单抗标记在氧化铁纳米颗粒的表面。免疫组化染色和磁共振扫描实验结果证明,此探针Fe3O4@DMSA@Ab对CD20阳性的人源淋巴瘤细胞Raji具有良好的靶向性。与单纯的利妥昔单抗和纳米颗粒组Fe3O4@DMSA相比,纳米探针Fe3O4@DMSA@Ab可有效降低Raji细胞活性,通过胞内Ca2+紊乱和活性氧增加促使线粒体膜电位降低,启动凋亡信号,抑制凋亡蛋白Bcl-2表达降低,促细胞凋亡蛋白Bax表达增加,诱导Raji细胞凋亡。同时,我们发现,磁场可以增强探针Fe3O4@DMSA@Ab对Raji细胞的促凋亡作用。
Lina Song, Wei Zhang, Hong Chen. Xizhi Zhang, Haoan Wu, Ming Ma, Zhongqiu Wang, Ning Gu, Yu Zhang., Apoptosis-promoting effect of rituximab-conjugated magnetic nanoprobes on malignant lymphoma cells with CD20 overexpression. International Journal of Nanomedicine, 2019:14 921–936.
https://doi.org/10.2147/IJN.S185458
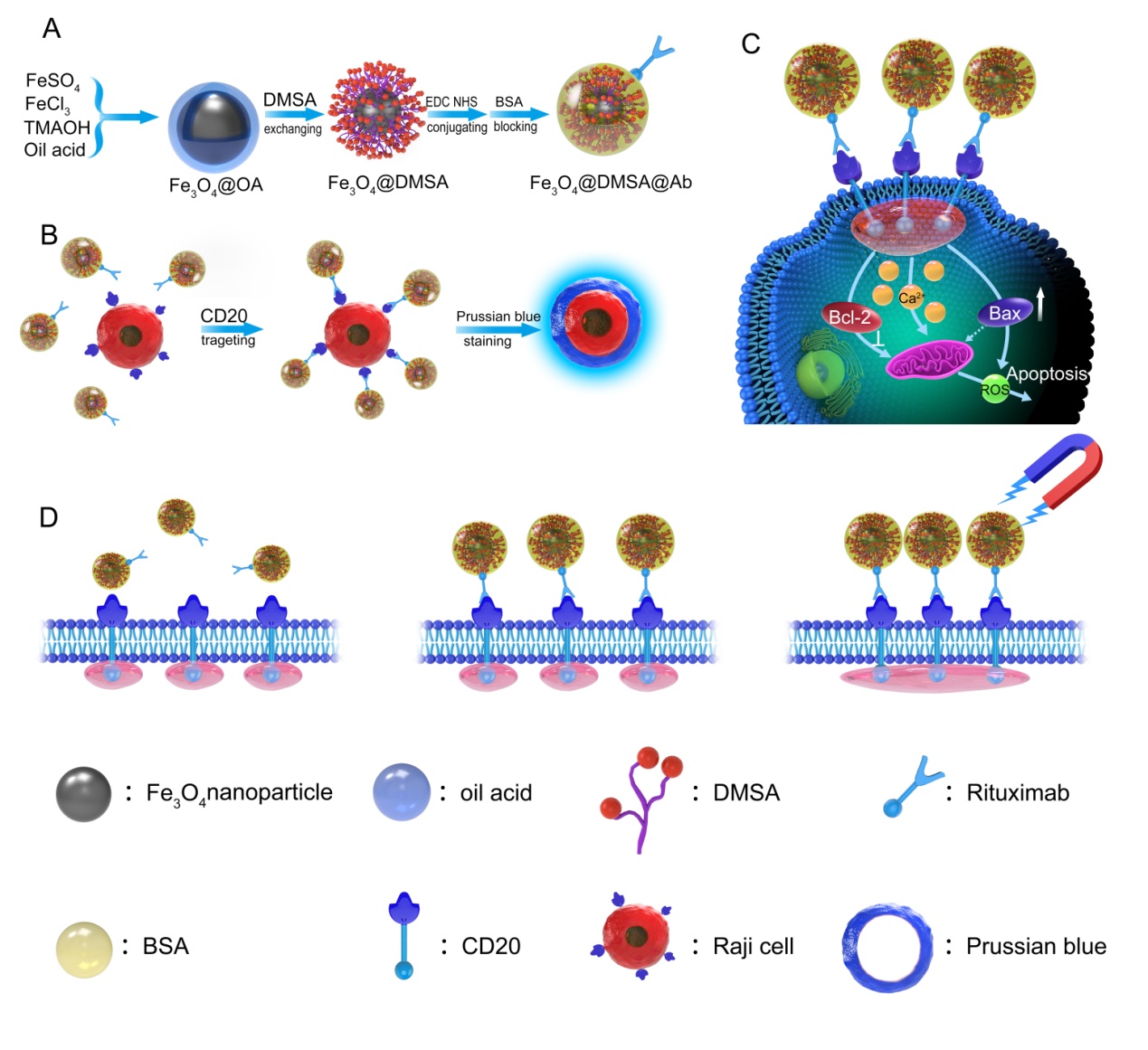
图1、纳米探针Fe3O4@DMSA@Ab的合成以及细胞作用示意图。
A、氧化铁Fe3O4@OA、Fe3O4@DMSA纳米颗粒和Fe3O4@DMSA@Ab纳米探针的合成步骤示意图;
B、纳米探针Fe3O4@DMSA@Ab标记在CD20阳性细胞Raji表面,通过普鲁士蓝染色显示;
C、南通探针Fe3O4@DMSA@Ab作用于细胞后,胞内信号变化;
D、磁场增强纳米探针Fe3O4@DMSA@ab诱导的细胞凋亡示意图;