胶质母细胞瘤(GBM)是一种高致死性的神经系统恶性肿瘤。手术治疗和放疗是临床上广泛使用的治疗方法,然而并未达到最佳的治疗效果,复发率高。为解决胶质母细胞瘤靶向性差、耐药性高等问题,本文构建了一种鞘氨醇1-磷酸修饰的靶向递送一氧化氮前体药物的脂质体(S1P/JS-K/Lipo)。S1P/JS-K/Lipo表现出GST/GSH响应的药物释放模式,有利于药物实现在肿瘤区域的释放。模拟血脑-肿瘤屏障(BBTB)存在的体外实验结果显示,较空白或仅载药的纳米载体而言,鞘氨醇1-磷酸修饰的前体药物脂质体可以增强小窝蛋白-1的跨膜递送,同时抑制P-gp蛋白的表达,这提高了纳米载体对于BBTB的渗透效率,进而增强诱导U87MG细胞死亡的效果。此外,U87MG细胞内逐渐产生的一氧化氮气体赋予了细胞超声成像的能力。体内实验结果显示,鞘氨醇1-磷酸修饰的前体药物脂质体表现出良好的胶质瘤成像效果,可以指示出U87MG细胞在原位胶质瘤模型鼠中的分布区域。此外,鞘氨醇1-磷酸修饰的前体药物脂质体可以阻止U87MG细胞向正常脑组织的浸润转移,延长GBM小鼠的生存期。该脂质体可以实现良好的BBTB渗透,和胶质瘤成像、治疗功能,为未来脑部肿瘤的靶向治疗提供了新思路。
该论文于2021年6月9日在线发表在Advanced Materials上:(Yang Liu, Xiao Wang, Jing Li, Jian Tang, Bin Li, Yu Zhang, Ning Gu*, Fang Yang*. Sphingosine 1-Phosphate Liposomes for Targeted Nitric Oxide Delivery to Mediate Anticancer Effects against Brain Glioma Tumors. Advanced Materials, 2021, 2101701. https://doi.org/10.1002/adma.202101701)
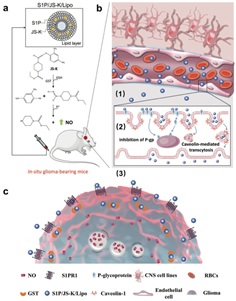
Figure Sphingosine 1-Phosphate Liposomes for Targeted Nitric Oxide Delivery to Mediate Anticancer Effects against Brain Glioma Tumors.