氧化铁纳米颗粒具有广泛的生物医学应用,但它们的潜在生物安全性问题仍然受到极大关注。尽管大量文献报道细胞在接触氧化铁纳米材料以后,会产生细胞凋亡/死亡、增殖/分化抑制,氧化应激水平升高等后果,但很少有研究直接关注纳米材料表面发生的化学反应,从而明确其毒性来源。
本文中我们发现氧化铁纳米颗粒具有pH依赖的类过氧化物酶和类过氧化氢酶双酶活性,并将其与细胞毒性联系起来。研究结果表明,在酸性条件下,氧化铁纳米颗粒能够催化H2O2产生羟自由基(•OH),进而氧化多种有机分子,即具有类过氧化物酶活性;而在中性条件下,氧化铁纳米颗粒直接催化双氧水分解为H2O和O2,即具有类过氧化氢酶活性。当被吞噬进入细胞以后,氧化铁纳米颗粒主要定位于酸性环境的溶酶体中,因而能通过类过氧化物酶活性增强H2O2诱导的细胞损伤。Fe3O4催化H2O2产生比Fe2O3更多的•OH,因而能够导致更强的细胞毒性。如果氧化铁纳米颗粒没有被困在溶酶体中,则可能不仅不会升高细胞内活性氧水平,反而能通过类过氧化氢酶活性达到抗氧化的目的。本文结果说明不同细胞内微环境对于氧化铁纳米颗粒的毒性可能具有相反的影响。考虑到细胞内源源不断产生的H2O2,逃避溶酶体的纳米颗粒运送方式可能是降低其长期细胞毒性的一种有效手段。
Zhongwen Chen, Jun-Jie Yin, Yu-Ting Zhou, Yu Zhang*, Lina Song, Mengjie Song, Sunling Hu, and Ning Gu*.
Dual Enzyme-like Activities of Iron Oxide Nanoparticles and Their Implication for Diminishing Cytotoxicity. ACS Nano, 2012. DOI:
10.1021/nn300291r.
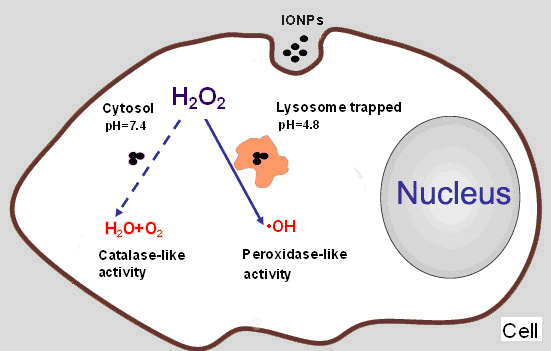
图1. 氧化铁纳米颗粒的双酶活性与其细胞毒性关系的示意图
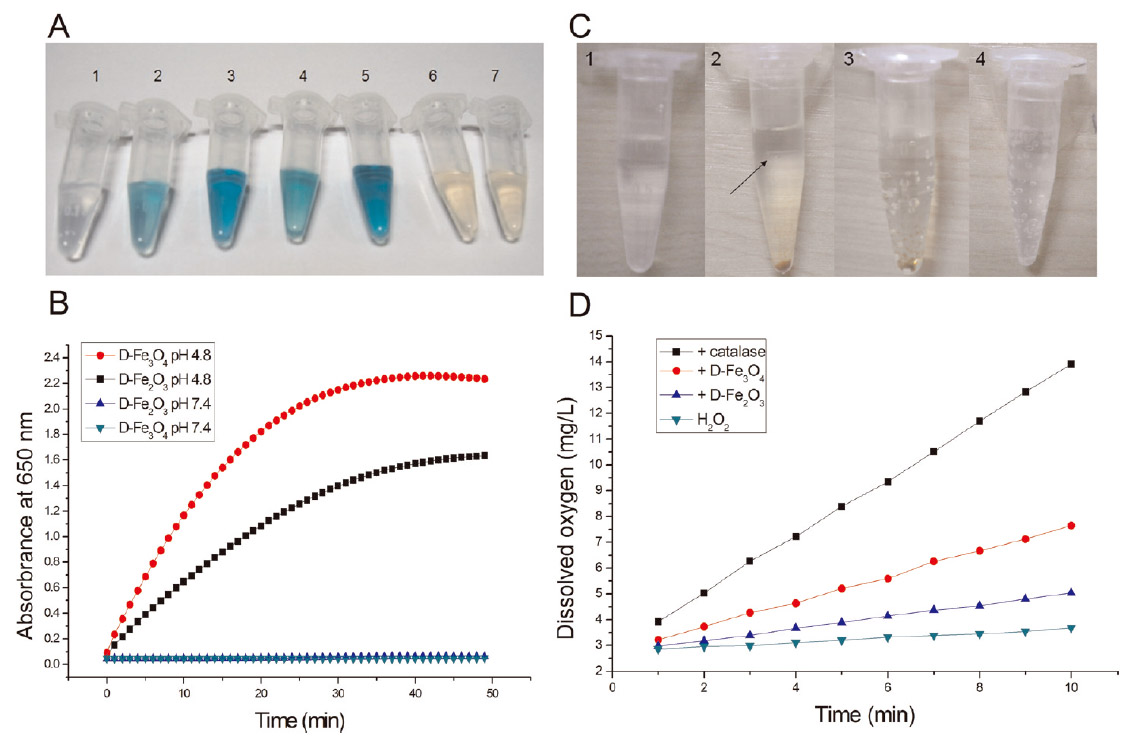
图2. 氧化铁纳米颗粒的双酶活性
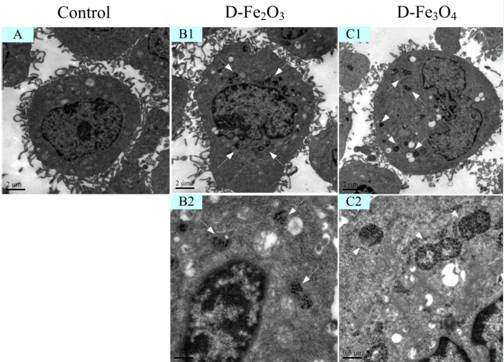
图3. 氧化铁纳米颗粒吞噬进入细胞后定位于内吞体或溶酶体中
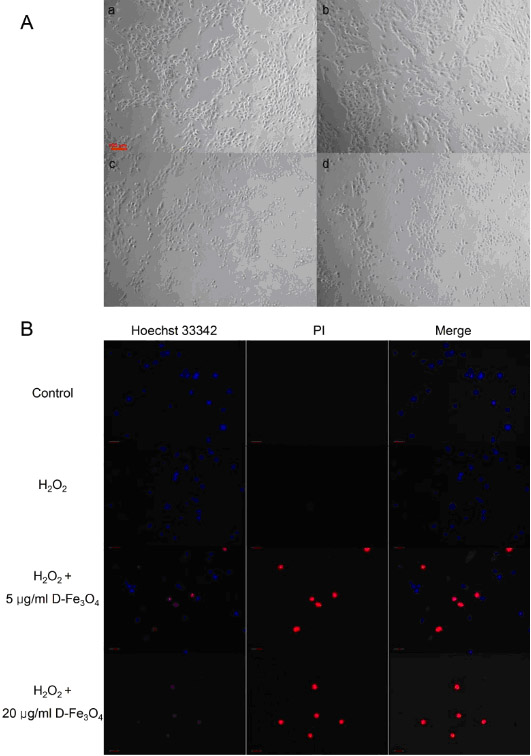
图4. 氧化铁纳米颗粒增强H2O2诱导的细胞损伤
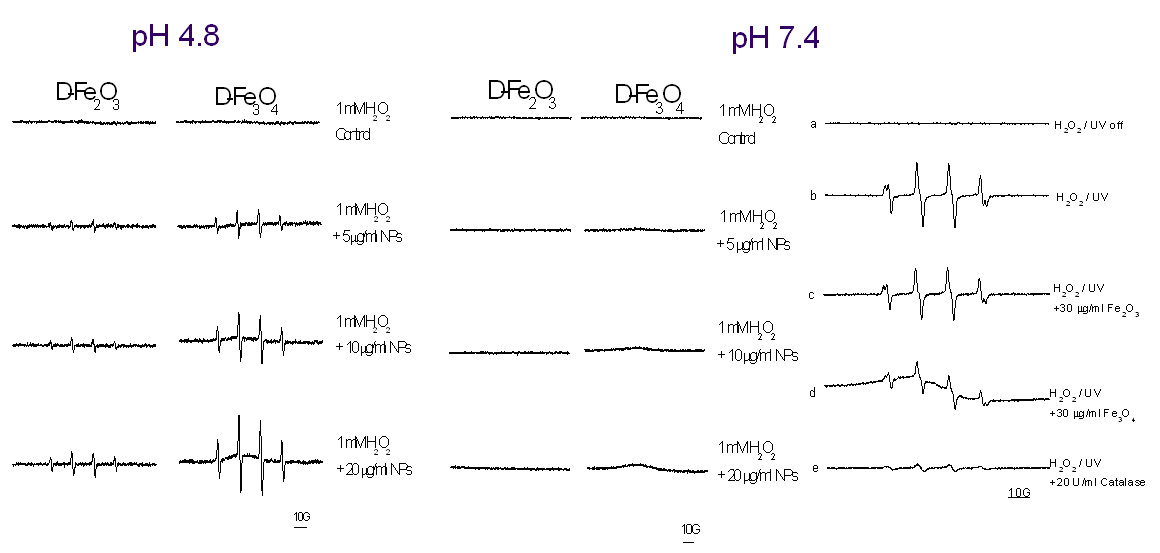
图5. 电子顺磁共振结合自旋标记技术验证氧化铁纳米颗粒在酸性环境中催化H2O2产生羟自由基,在中性环境中催化H2O2分解为水和氧气